青木生物技术(武汉)有限公司代理商
7 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.5
- 0.5
- 2.5
- 2.5
文献支持
CRISPR Cas12a DNA检测试剂盒 (二步法)(液体)(恒温-试纸型)
¥3000
代理商
青木生物技术(武汉)有限公司
入驻年限:7 年
- 联系人:
刘经理
- 所在地区:
湖北 武汉市 洪山区
- 业务范围:
体外诊断、细胞库 / 细胞培养、试剂、抗体、ELISA 试剂盒、实验室仪器 / 设备
- 经营模式:
代理商 经销商 生产厂商
推荐产品
公司新闻/正文
SARS-CoV-2 抗原检测: 检测安全性探讨
4958 人阅读发布时间:2022-04-26 17:48
唾液或鼻咽拭子测试对于呼吸道疾病的病原体检测至关重要,未来将越来越多地用于 Covid 疫苗接种后的免疫检测。在这种情况下,鼻咽拭子或唾液样本的潜在高传染性通常会导致用户危险和相关的监管障碍。然而,对于唾液和鼻咽拭子检测如 SARS-CoV-2 抗原快速检测,安全设计如采用 SafetyTector™ S 病毒灭活缓冲液则能很容易即可实现。
此外,唾液也被证明适合作为样本类型,用于在血清学测试中检测 SARS-CoV-2 特异性 IgG 抗体。因此,由 IgA 抗体介导的所谓「粘膜免疫」也很容易测量。这有助于防止免疫个体变得具有传染性。唾液样本也是检测针对其他病原体的抗体的良好样本类型,因为结果与血清学血清测试的结果相关性很好。基于唾液的检测系统其主要优势是为患者采集样本的简易性和便利性,尤其是对于非专业人员使用时。
然而,在 SARS-CoV-2 大流行的背景下,这些检测系统的缺点也变得明显:一般而言,患者样本必须始终被认为具有潜在的传染性。在呼吸道病毒大流行的传播时期,这个问题更加严重,因为受感染的个体在出现症状前就已经具有传染性,无症状感染也很常见。世卫组织建议病毒灭活前在生物安全柜中处理样本以检测 SARS-CoV-2。然而,这些检测是在学校、幼儿园、疗养院和工作场所进行的,没有足够的防护措施,更不用说安全柜了。
这对体外诊断产品的生产商来说尤其是个问题。降低对用户的风险是验证新开发诊断产品的强制性部分。ISO 14971,「风险管理在医疗器械中的应用」,管理 ISO 13485 的实施,规定医疗器械的设计和制造应具有本质安全 (安全设计)。欧盟自 2022 年 5 月 26 日起强制执行的体外诊断法规也要求生产商「通过安全设计和制造尽可能消除或降低风险」。 仅当根据现有技术无法做到这一点时,保护措施或安全信息才是可接受的降低风险的手段 (see Fig. 1)。
用于呼吸道样本 PCR 诊断的提取缓冲液通常是病毒灭活的,因此符合安全设计的要求。而另一方面,抗原检测通常使用温和的缓冲液,不一定能灭活 SARS-CoV-2。因此,目前用于快速检测的许多稀释剂没有足够的灭活效果。多余的标本和测试盒在测试后仍然具有传染性,并对健康构成威胁。特别是在大流行中进行大规模检测的场所,这是完全不必要的危险情况,可以通过使用病毒灭活稀释缓冲液来避免。然而,不幸的是,正是安全设计方法的这一要素在市场上许多抗原试验的发展中被忽视或没有得到充分的证明。即使声称有病毒灭活作用,也只有在极少数情况下,才在生物安全 3 级((BSL-3) 实验室用真正的病毒分离物进行了有意义的实验来证实。但是,如果没有足够的数据,就无法要求或保证用户保护。如果没有证据,审计师就无法做出积极的决定来准许诊断产品投放市场。
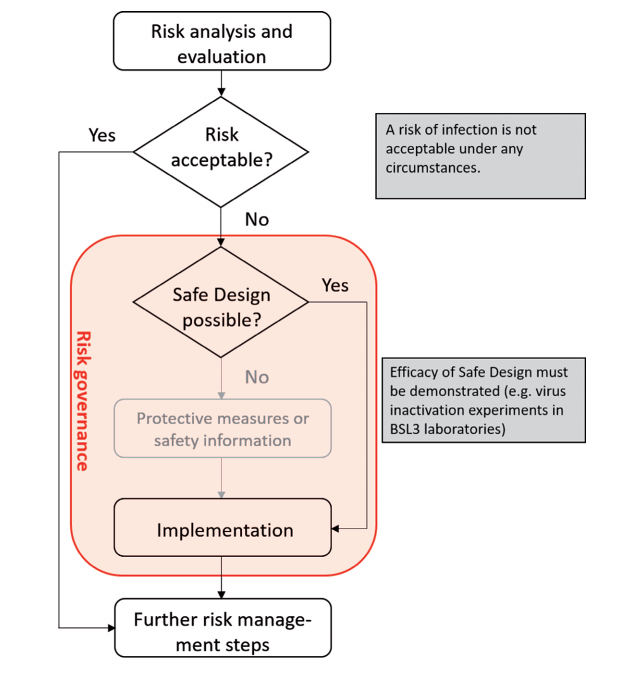
Fig.1:根据 ISO 14971 确定风险控制选项的优先级。如果可行,医疗器械应设计为本质安全(安全设计)。只有在不可能的情况下,
才可接受通过保护措施或安全信息作为风险控制措施。因此,对于用户保护,病毒灭活缓冲液比保护措施(如手套、护目镜、防
撕收集袋)或安全信息(如产品说明书)更可取。
解决方案: SafetyTectorTMS
为了解决病毒灭活的问题,使所有市场参与者无需投入大量金钱和时间就能获得安全的稀释缓冲液,CANDOR 开发出了 SafetyTector™ S 。SafetyTector™ S 是一种即用型的病毒灭活稀释液和提取缓冲液,用于唾液样本和鼻咽拭子。同时,SafetyTector™ S 不是有害物质。此外,病毒灭活效果是在不使用对环境有害的灭活病毒成分的情况下实现的。例如常用的内分泌干扰物 Triton X-100。Triton X-100 不得再用于许多国际市场的产品。
为了保证使用者的安全,病毒灭活效果必须经过实验验证。在乌尔姆大学医学中心的 BSL3 生物安全实验室中,Dr. Jan Münch 教授的团队对唾液稀释液中的 SARS-CoV-2、甲型流感病毒 (infuenza A virus ) 和单纯疱疹病毒 1(herpes simplex virus 1) 进行传染性分离测试。结果显示,与 SafetyTectorTM S 孵育了仅 1 分钟后,即未检测到残留感染性 (Fig. 2)。与其他人类病原体的测试中也获得了可比性的结果。如麻疹病毒 (measles virus)、单纯疱疹病毒 (herpes simplex virus 2)、寨卡病毒 (Zika virus) 及 SARS-CoV-2 变异株 B.1.1.7 (「英国变异株」) 和 B.1.351 (「南美变异株」)。
因此,SafetyTector™ S 具有广谱的抗病毒作用,可降低在分析潜在患者唾液和鼻咽拭子样本时的风险。
为了解决病毒灭活的问题,使所有市场参与者无需投入大量金钱和时间就能获得安全的稀释缓冲液,CANDOR 开发出了 SafetyTector™ S 。SafetyTector™ S 是一种即用型的病毒灭活稀释液和提取缓冲液,用于唾液样本和鼻咽拭子。同时,SafetyTector™ S 不是有害物质。此外,病毒灭活效果是在不使用对环境有害的灭活病毒成分的情况下实现的。例如常用的内分泌干扰物 Triton X-100。Triton X-100 不得再用于许多国际市场的产品。
为了保证使用者的安全,病毒灭活效果必须经过实验验证。在乌尔姆大学医学中心的 BSL3 生物安全实验室中,Dr. Jan Münch 教授的团队对唾液稀释液中的 SARS-CoV-2、甲型流感病毒 (infuenza A virus ) 和单纯疱疹病毒 1(herpes simplex virus 1) 进行传染性分离测试。结果显示,与 SafetyTectorTM S 孵育了仅 1 分钟后,即未检测到残留感染性 (Fig. 2)。与其他人类病原体的测试中也获得了可比性的结果。如麻疹病毒 (measles virus)、单纯疱疹病毒 (herpes simplex virus 2)、寨卡病毒 (Zika virus) 及 SARS-CoV-2 变异株 B.1.1.7 (「英国变异株」) 和 B.1.351 (「南美变异株」)。
因此,SafetyTector™ S 具有广谱的抗病毒作用,可降低在分析潜在患者唾液和鼻咽拭子样本时的风险。
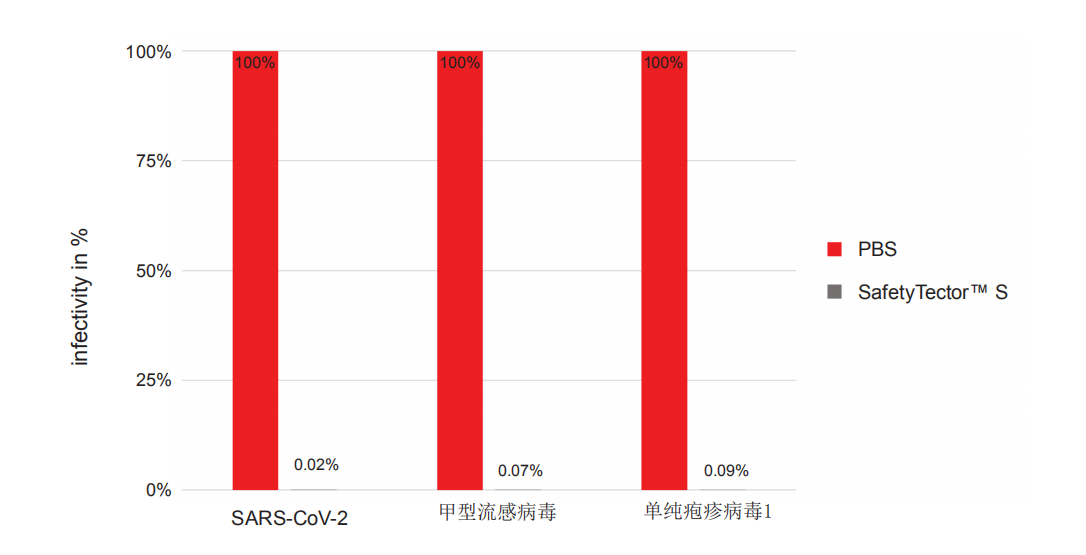
Fig.2: SafetyTector™ S 具有广谱的抗病毒作用。掺入 SARS-CoV-2、甲型流感病毒 (infuenza A virus) 或单纯疱疹病毒 1 (HSV-1)的唾液样本分别与 PBS、
CANDOR 的 SafetyTector™ S 按照 1:4 比例混合,室温孵育 1 分钟 (n = 3)。孵育后,样本进行滴定并被加入到 Vero E6 (SARS-Cov-2 和 HSV-1) 、MDCK (infuenza
A virus)细胞中进行培养。4-7 天后,采用 Reed-Muench 法测定病毒感染性。结果显示,对于所有测试的三种病毒,使用此方法与 SafetyTector™ S 孵育后,均不再检测到感染性。
CANDOR 的 SafetyTector™ S 按照 1:4 比例混合,室温孵育 1 分钟 (n = 3)。孵育后,样本进行滴定并被加入到 Vero E6 (SARS-Cov-2 和 HSV-1) 、MDCK (infuenza
A virus)细胞中进行培养。4-7 天后,采用 Reed-Muench 法测定病毒感染性。结果显示,对于所有测试的三种病毒,使用此方法与 SafetyTector™ S 孵育后,均不再检测到感染性。
分析性能评价
除了对使用者安全之外,强大的分析性能对诊断试剂盒的开发和验证也是必不可少的。选择合适的稀释液对性能至关重要。分析潜在感染样本的一个挑战是如何产生病毒灭活效果但不干扰抗原-抗体相互作用而导致错误结果。CANDOR 在开发区 SafetyTector™ S 的过程中实现了这种平衡。在德国联邦药物和医疗器械研究所 (BfArM) 列出的市售快速抗原测试中,通过用 SafetyTector™ S 替换各自提供的稀释和提取缓冲液来研究分析性能。在这些不同的快速抗原测试中,当使用SafetyTector™ S 时,检测限保持不变且没有假阳性结果产生 (Fig. 3 A - D)。虽然快速检测试剂盒不是用 SafetyTector? S 开发的,但 SafetyTector™ S 与原始稀释液相当。通过将 SafetyTector™ S 纳入基于唾液或鼻咽拭子的免疫测定的开发和优化中,可以在不影响分析性能的情况下解决使用者安全问题。
此外,SafetyTector™ S 的成分能够改善许多唾液样本经常出现的质地和粘度的问题,从而改善其流动特性,这在基于流体学的免疫测定中是一个优势,如侧向层析检测。
此外,SafetyTector™ S 的成分能够改善许多唾液样本经常出现的质地和粘度的问题,从而改善其流动特性,这在基于流体学的免疫测定中是一个优势,如侧向层析检测。

Fig.3: SafetyTector™ S 与来自不同生产商的快速抗原测试兼容。来自健康供体的唾液样本未经处理 (阴性样本) 或添加 SARS-
CoV-2 抗原 (阳性样本) 后,根据产品说明书,使用提供的稀释缓冲液 (Standard Buffer) 或 SafetyTector™ S。
生产商:A) DRG Instruments; B) Roche; C) BTNX; D) Abbott
CoV-2 抗原 (阳性样本) 后,根据产品说明书,使用提供的稀释缓冲液 (Standard Buffer) 或 SafetyTector™ S。
生产商:A) DRG Instruments; B) Roche; C) BTNX; D) Abbott
SafetyTector? S - 免疫分析新进展
CANDOR 开发的 SafetyTector™ S 是一种用于免疫测定中的稀释和提取缓冲液,可以灭活唾液或鼻咽拭子样本中包含的病毒,从而显著提高体外诊断的用户安全性。且诊断的分析性能仍维持高水平不变。因此,SafetyTector™ S 展现了一种新的免疫分析进展。SafetyTector™ S 的使用节省了诊断免疫测定的研发、风险管理和验证方面的资源和时间。基于该技术的测定也可由非专业人士在学校等社区环境中进行安全地进行。此外,正确处理使用过的检测试剂盒对使用者来说也不再是一个挑战。
CANDOR 位于德国旺根的经 EN ISO 13485 认证的生产设施保证了 SafetyTector™ S 始终如一的高品质,并且可实现高达 1000L 的批量生产。可应要求为体外诊断的开发商和生产商提供 SafetyTector™ S 测试样本。
CANDOR 位于德国旺根的经 EN ISO 13485 认证的生产设施保证了 SafetyTector™ S 始终如一的高品质,并且可实现高达 1000L 的批量生产。可应要求为体外诊断的开发商和生产商提供 SafetyTector™ S 测试样本。
文献引用:
1、Teo,AKJ et al. (2021) Saliva is more sensitive than nasopharyngeal or nasal swabs for diagnosis of asymptomatic and mild
COVID-19 infection. Nature Scientifc Reports
2、MacMullan,MA et al. (2020) ELISA detection of SARS-CoV-2 antibodies in saliva. Nature Scientifc Reports
3、Hettegger,P et al. (2019) High similarity of IgG antibody profles in blood and saliva opens opportunities for saliva based
serology. PLoS One
4、World Health Organization (2020) Laboratory biosafety guidance related to coronavirus disease (COVID-19)
5、EN ISO 14971:2019,Annex A,Section A.2.7.1 Risk Control Option Analysis
6、Regulation (EU) 2017/746,Annex I,Chapter I,paragraph 4 (In-vitro-Diagnostics Regulation)
7、Public Health England (2020) COVID-19:PHE laboratory assessments of inactivation methods
8、List of substances included in Annex XIV of REACH (?Authorisation List「),Entry 4-(1,1,3,3-tetramethylbutyl)phenol,etho-xylated (https://www.echa.europa.eu/web/guest/authorisation-list/-/dislist/details/0b0236e1807df80d)
COVID-19 infection. Nature Scientifc Reports
2、MacMullan,MA et al. (2020) ELISA detection of SARS-CoV-2 antibodies in saliva. Nature Scientifc Reports
3、Hettegger,P et al. (2019) High similarity of IgG antibody profles in blood and saliva opens opportunities for saliva based
serology. PLoS One
4、World Health Organization (2020) Laboratory biosafety guidance related to coronavirus disease (COVID-19)
5、EN ISO 14971:2019,Annex A,Section A.2.7.1 Risk Control Option Analysis
6、Regulation (EU) 2017/746,Annex I,Chapter I,paragraph 4 (In-vitro-Diagnostics Regulation)
7、Public Health England (2020) COVID-19:PHE laboratory assessments of inactivation methods
8、List of substances included in Annex XIV of REACH (?Authorisation List「),Entry 4-(1,1,3,3-tetramethylbutyl)phenol,etho-xylated (https://www.echa.europa.eu/web/guest/authorisation-list/-/dislist/details/0b0236e1807df80d)